在肿瘤微环境中,调节性T(regulatory T,Treg)细胞起到免疫抑制的作用,在许多肿瘤中Treg细胞大量浸润从而造成肿瘤组织的免疫逃逸,会对治疗和预后产生不良影响。CCR8(CC chemokine receptor 8,CCR8)属于CC族趋化因子受体家族,其主要在肿瘤微环境中的Treg细胞上特异性高表达,而在周围正常组织和外周血中低表达,因此CCR8可以作为Treg细胞的一种特异性标志物,是一种有潜力的治疗靶点和生物标志物。近年来多项研究表明,CCR8+Treg细胞耗竭策略是未来抗癌的一种可选方案,并且通过与其他免疫治疗药物联用,靶向表达CCR8的Treg细胞可以有效地减少肿瘤微环境中浸润淋巴细胞的免疫抑制,通过发掘CCR8的潜在功能将会显著提升免疫治疗的效果。
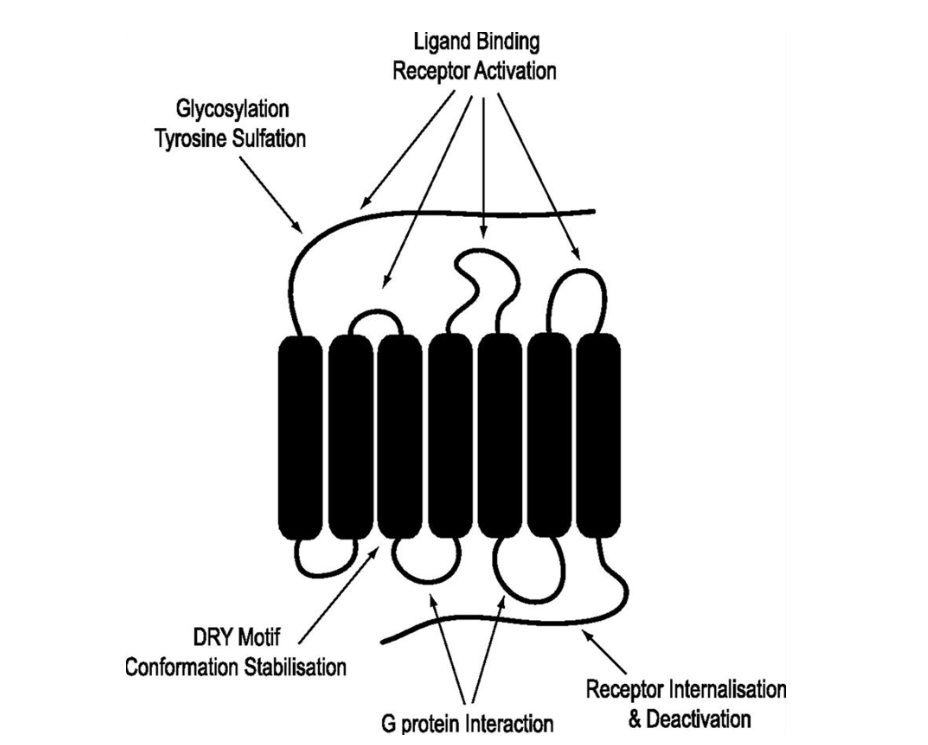
图1.CCR8结构图[1]
肿瘤免疫靶点-CCR8
CCR8(Chemokine receptor 8)是一种七次跨膜G蛋白偶联受体,属于趋化因子受体C-C亚家族。与其他趋化因子受体一样,CCR8与其配体结合后可以导致一系列的细胞反应,包括趋化因子典型的趋化反应和非典型的炎症反应等。CCR8参与Treg和Th2细胞向炎症和肿瘤部位的募集, 其高表达与多种癌症相关,包括结直肠癌、乳腺癌、胃癌、转移性脑癌、转移性肝癌等,被认为是肿瘤部位Treg的潜在特异性标记物,是极具潜力的肿瘤免疫靶点。
CCR8配体
人源CCR8有四种已知配体:CCL1、CCL8、CCL16和CCL18,其中CCL1为其主要配体。CCR8是目前已知CCL1的唯一受体。CCR8 与其配体的相互作用参与了多种肿瘤的发展进程及介导了肿瘤的免疫逃逸。
CCR8作用机制
CCL1是一种由T淋巴细胞,单核细胞等分泌的小分子糖蛋白,CCL1被释放到肿瘤微环境中后,一方面可以激活肿瘤细胞上的CCR8受体,实现癌细胞的增殖、迁移和凋亡抵抗,因此药物研发可以通过阻断CCL1/CCR8途径来增强抗肿瘤免疫作用。
另一方面,CCL1可以募集Treg细胞到肿瘤生态位,并导致CD4+T细胞转化为Treg。因此CCR8 治疗性抗体的作用机理除了单纯的功能阻断,也可通过 ADCC 效应耗竭肿瘤浸润的 FOXp3+ CCR8+ Treg细胞,以增强抗肿瘤免疫。
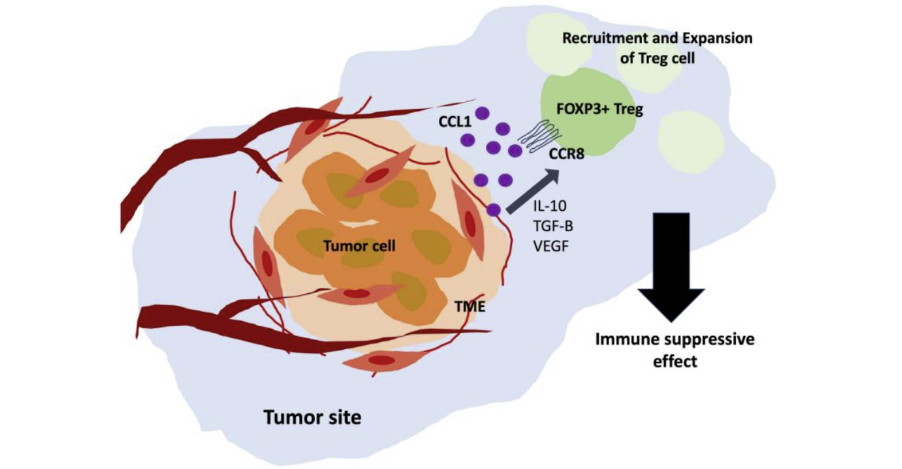
图2 .CCL1–CCR8 相互作用的信号传导[2]
CCR8其他配体CCL8、CCL16和CCL18。CCL8可以作为一种生物标志物,与PD-1的表达、局部M2巨噬细胞浸润呈正相关。CCL16则主要在肝脏和肝癌细胞中表达,可以与CCR1相互作用促进癌细胞的肝转移。CCL16也可增强细胞毒性T淋巴细胞和树突状细胞的抗癌作用。CCL18主要存在于人体的肺部和血清中,主要与过敏反应、肿瘤细胞激活和迁移有关,并且通过直接刺激免疫细胞来影响免疫功能和促进Treg细胞的产生。
CCR8药物在研管线
全球范围内有至少十余款处于临床试验和临床前阶段的CCR8靶向药物研发管线。但目前,尚无CCR8靶点药物获批上市。其中,百时美施贵宝的 BMS-986340、盐野义制药的 S-531011 以及礼新医药的 LM-108 研发进展领先。其他处于在研状态的 CCR8 靶向药达到数十款。
01
百时美施贵宝的BMS-986340
全球第一款开展临床试验的CCR8靶向性单克隆抗体,通过去岩藻糖基化增强抗体依赖的细胞介导的细胞毒性作用(ADCC)。
02
礼新医药的LM-108
靶向CCR8的单抗,能够通过ADCC特异性清除肿瘤Treg细胞来调节肿瘤微环境,同时不影响外周Treg。于2022年5月获批临床。
03盐野义制药的S-531011 Shionogi开发的新型抗人IgG1抗体,在肿瘤浸润Tregs中选择性表达,对表达CC-+R8的细胞具有体外抗体依赖性细胞毒性,并对CCL1-CCR8信号通路具有中和活性。04和铂医药的HBM1022 CCR8单抗,HBM1022与CCR8特异性结合后可以清除肿瘤微环境内的Treg细胞,呈现出显著的抗肿瘤效果,同时与抗PD-1抗体具有潜在的良好协同作用。05艾美斐的IPG7236 靶向CCR8的小分子抑制剂。CCR8小分子抑制剂不仅能够抑制肿瘤细胞转移,也可以抑制肿瘤相关Treg细胞向肿瘤组织浸润,从而逆转肿瘤免疫抑制性微环境,增强抗肿瘤免疫反应。
除此之外,还有一些针对靶向CCR8药物的研究。
全长跨膜蛋白新品:CCR8蛋白
具有全长完整结构的多次跨膜蛋白在药物研发中具有重要意义。为助力跨膜蛋白靶点药物的开发,翌圣生物开发出基于哺乳细胞的病毒样颗粒(VLPs)表达跨膜蛋白技术平台,该技术平台所制备的多次跨膜蛋白,具备完整的生物活性。全长CCR8-VLP蛋白保留了蛋白的天然构象,使药物筛选更精准,更好的激活体液和细胞免疫反应。并且全长蛋白的表达也有助于揭示其在免疫调节和肿瘤微环境中的作用机制。
YEASEN基于HEK293表达系统的包膜VLP技术平台,已成功开发出七次全长跨膜蛋白CCR8,为靶向CCR8药物研发提供支持。
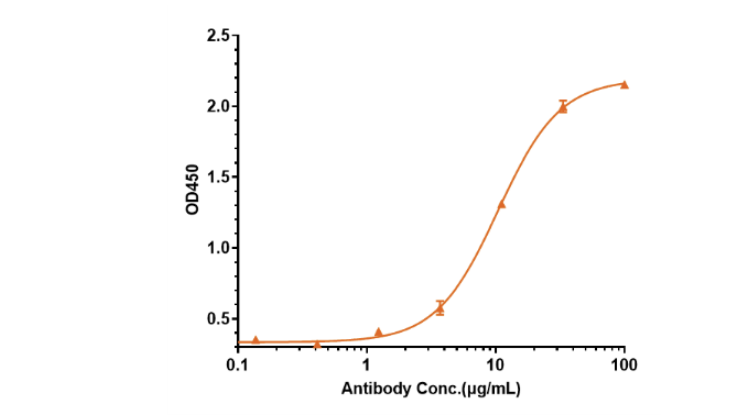
全长CCR8(VLP)蛋白验证数据
相关产品推荐
|
产品名称 |
货号 |
规格 |
|
95037ES |
20μg/100μg/1mg |
参考文献:
1. White G E., et al. (2013). CC chemokine receptors and chronic inflammation-therapeutic opportunities and pharmacological challenges. Pharmacological reviews, 65(1), 47-89.
2. Nari Kim,et al.CCR8 as a Therapeutic Novel Target: Omics-Integrated Comprehensive Analysis for Systematically Prioritizing Indications. Biomedicines. 2023 Nov; 11(11): 2910.
