Arjen Gerssen1、Mirjam D. Klijnstra1、Simon Cubbon2和Antonietta Gledhill2
1瓦格宁根大学食品安全研究所(荷兰瓦格宁根)
2沃特世公司(英国曼彻斯特)
应用优势
这是一种能够快速、可靠地分析贝类中管制和非管制亲脂性海洋生物毒素的方法。与传统的HPLC/MS/MS方法相比,其分析速度提高了4倍:(单次分析由20 min缩短为5 min)。本方法还可以满足规定的检测水平,可用于代替小鼠生物检测法。
沃特世解决方案
ACQUITY UPLC® 系统
ACQUITY UPLC BEH C18色谱柱
Xevo® TQ-S质谱仪
TargetLynx™ 应用软件
QUANPEDIA™ 数据库
关键词
贝类,生物毒素,亲脂性,藻毒素,贻贝,蛤,牡蛎,腹泻性贝毒,DSP
简介
食用受到生物毒素污染的贝类(贻贝、牡蛎、蛤等)可能会引起人体严重中毒,如腹泻性贝毒(DSP)。由于DSP毒素具有亲脂性,通常将其归类为亲脂性海洋生物毒素。海洋生物毒素由不同种类的浮游植物自然产生,因此也称之为藻毒素。亲脂性海洋生物毒素在理化性质方面呈现出多样性,如羧酸、磺酸、氨基和亚氨基官能团,因此具有一定的复杂性。
欧盟(EU)立法对各种类别的毒素进行管制,并在官方控制程序中具体介绍了对这些毒素实施监控的方式。如图1A所示,应当受到监控的亲脂性生物毒素有冈田软海绵酸(OA);鳍藻毒素1、2、3(DTX1,2,3),其中DTX3分别是OA,DTX1和2的酯类形式;扇贝毒素1、2(PTX1,2);虾夷扇贝毒素(YTX);45OH虾夷扇贝毒素(45OH YTX);同源虾夷扇贝毒素(homoYTX);45OH同源虾夷扇贝毒素(45OH homoYTX);原多甲藻酸1、2和3(AZA1,2,3)1 。
在2011年7月之前,上述毒素的官方检测方法为一种生物检测法,该方法基于大鼠口服贝类肉或小鼠腹腔注射贝类提取物进行检测。这种方法主要存在两个问题:第一,有违生物伦理学;第二,无法非常科学地、可靠地测定痕量的特定毒素。
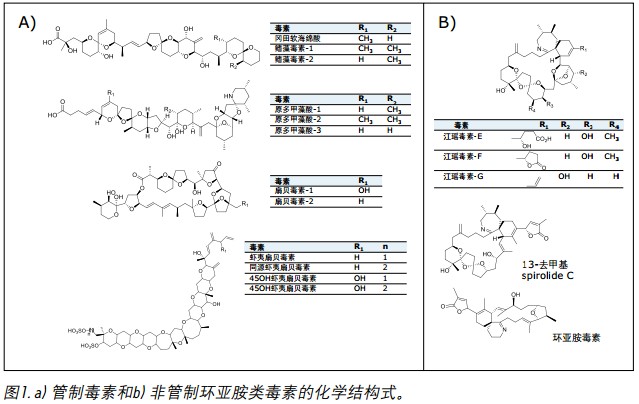
采用生物检测法进行检测时,环亚胺类毒素的存在会引起一种物理反应,通常使动物致死。环亚胺类毒素如图1B所示,根据理化性质也被归类为亲脂性海洋毒素。虽然这些毒素目前尚未受到管制,但欧洲食品安全局(EFSA)指出,这类毒素的毒性数据以及其贝类中的存在情况应当被更多地收集。
自2011年7月起,LC/MS/MS成为贝类中亲脂性海洋生物毒素的官方检测方法2。欧盟引用的LC/MS/MS方法是使用固定的提取步骤提取生物毒素,再通过传统LC方法在酸性或碱性流动相下进行分离,并使用串联四极杆MS进行检测。
本次研究的目的是建立一种在碱性条件下比传统LC方法更快速的常规分析方法,其中还包括EFSA关注的其他非管制类化合物的分析。在本应用纪要中,我们使用Waters® ACQUITY UPLC系统串联Xevo TQ-S质谱仪,对包括部分非管制环亚胺类毒素在内的多种亲脂性海洋生物毒素进行了为时五分钟的检测分析。UPLC® 技术能够缩短分析运行时间,并且不会对色谱峰分离度和峰质量产生不良影响,而Xevo TQ-S(串联四极杆质谱仪)可提供超高灵敏度的检测,还能够在切换电喷雾正离子(ESI+)和负离子(ESI-)模式下同时采集多重反应监测(MRM)跃迁数据,该采集过程是分析亲脂性海洋生物毒素的必需步骤。
下载完整应用纪要请点击:http://www.waters.com/waters/library.htm?cid=511436&lid=134726092&locale=zh_CN
